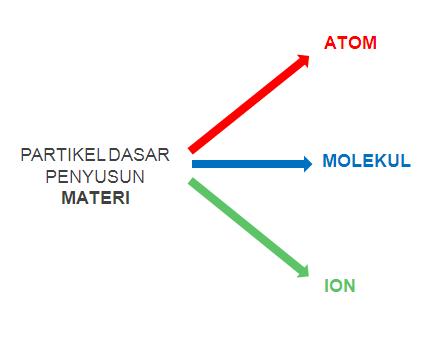
Partikel adalah sebuah satuan dasar dari benda atau materi. Bisa juga dikatakan Partikel merupakan satuan bagian terkecil dari suatu materi. Jenis Partikel ini ada 3 yaitu: atom, molekul, dan ion. Jadi baik atom, molekul, dan ion ke tiga-nya merupakan satuan terkecil dari materi yg secara umum disebut partikel
1. Atom adalah: Satuan terkecil dari suatu materi yang terdiri atas inti, yang biasanya mengandung proton (muatan+) dan neutron (netral), dan kulit yang berisi muatan negatif yaitu elektron. Ada juga yang menyebutkan bahwa atom adalah partikel penyusun unsur.
Kedua pengetian ini semuanya benar. Yang pasti atom itu :
– punya proton, neutron, elektron, (kecuali pd Hidrogen-1, yg tidak memiliki neutron)
– punya karekteristik tertentu, yaitu punya jumlah proton dan elektron yang sama (jika tdk sama disebut ion)
– atom2 yang punya karakteristik yang sama dinamakan unsur,
Analogi sederhana: Setiap orang yang sering membaca, kita sebut sikutu buku, ceritanya kita punya 4 teman yang punya hobi membaca, sehingga kita simpulkan keempat teman kita ini sikutubuku karena punya kebiasaan yang sama. Jadi
teman kita= atom,
sama2 hobi baca= punya jumlah proton&elektron sama/ berkarakter sama,
sikutu buku=unsur
Anggapan yang salah
– gabungan/ikatan beberapa atom akan membentuk unsur (SALAH).
Yang benar: unsur adalah nama untuk kumpulan/himpunan atom yang punya karakter yang sama. Gabungan/ikatan dari beberapa atom bukan membentuk unsur tapi membentuk molekul. Bedakan himpunan dan ikatan..!
2. Molekul adalah: Gabungan dari beberapa atom unsur, bisa dua atau lebih. Artinya ketika berbicara molekul maka yang dibayangkan adalah gabungan atom2 (bukan 1 atom). Molekul adalah partikel terkecil dari suatu unsur/senyawa
– Jika gabungan dari atom unsur yang sama jenisnya maka disebut Molekul Unsur, Contohnya: O2, H2, O3, S8
– Jika gabungan dari atom unsur yang berbeda jenisnya maka disebut Molekul Senyawa, Contohnya: H2O, CO2, C2H5
3. Ion adalah: atom yang bermuatan listrik, ion yang bermuatan listrik disebut kation, dan ion yang bermuatan negatif disebut anion. Kation dan anion dapat berupa ion tunggal hanya terdiri dari satu jenis atom atau dapat pula berupa ion poliatom mengandung dua atau lebih atom yang berbeda.
Beberapa Kesimpulan:
Unsur itu partikelnya bisa berupa atom/molekul unsur. Unsur2 yang partikelnya berupa atom, berarti unsur tersebut bisa berdiri sendiri atau hanya mengandung satu atom saja, penulisannya ditulis dengan lambang unsurnya, misalnya C (karbon), He (Helium). Bila partikelnya berupa molekul maka artinya unsur tersebut dibentuk dari gabungan atom yang berjenis sama, dia tidak bisa berdiri sendiri, unsur2 tersebut ditulis dengan lambang unsurnya disertai dengan jumlah atom penyusunya. Contohnya: O2, H2. Makanya unsur oksigen tidak pernah ditulis hanya huruf O saja, melainkan ditambah angka 2 sebagai arti bahwa Unsur ini dibentuk dari 2 atom oksigen.
JENIS-JENIS MATERI/ZAT
Materi/Zat secara umum dibagi menjadi 2 bagian yaitu zat tunggal dan campuran. Zat tunggal dapat berupa unsur, atau berupa senyawa. Sedangkan campuran dapat berupa campuran homogen atau berupa campuran heterogen.
1. Unsur adalah: Sekelompok atom yang memiliki jumlah proton yang sama pada intinya. Jumlah ini disebut sebagai nomor atom unsur. Unsur didefinisikan pula sebagai zat tunggal yang sudah tidak bisa dibagi-bagi lagi menjadi bagian yang lebih kecil.
Saya hanya ingin menekankan “unsur hanyalah sebutan saja untuk atom-atom yg yang punya karakter sama (punya jumlah proton yg sama)”. Sebagai contoh, semua atom yang memiliki 6 proton pada intinya adalah atom dari unsur kimia karbon, dan semua atom yang memiliki 92 proton pada intinya adalah atom unsur uranium.Bisa dibilang unsur adalah atom itu sendiri, contohnya: jika ada H2O, maka kita bisa bilang: terdiri dari 2 atom hidrogen, dan 1 atom oksigen, padahal Hidrogen dan oksigen keduanya adalah unsur.
2. Senyawa: Senyawa adalah zat tunggal yang terdiri atas beberapa unsur yang saling kait-mengait. Senyawa dibentuk dari minimal 2 unsur yang berbeda. Walaupun dibentuk dari unsur yang berbeda, namun senyawa tetap disebut zat tunggal, karena sifat-sifat unsur yang membentuknya tidak dapat di temukan pada senyawa. Dengan kata lain
Senyawa telah menjelma menjadi zat yang baru.Contoh:
Reaksi antara Hidrogen(H) dan oksigen (O2), diperoleh zat baru yang disebut air, yaitu:
H + O2 ——–> H2O
Pada reaksi tersebut, dihasilkan zat baru yang sifatnya berbeda dari unsur-unsur penyusunnya. Hidrogen adalah gas yang sangat ringan dan mudah terbakar, sedangkan oksigen adalah gas yang terdapat di udara yang sangat diperlukan tubuh kita untuk pembakaran. Tampak jelas bahwa sifat air berbeda dengan sifat hidrogen dan oksigen.
Ciri khas senyawa adalah dia mempunyai perbandingan massa penyusun yang tetap, air tersusun dari oksigen dan hidrogen dengan perbandingan massa unsur oksigen banding hidrogen adalah selalu 8 : 1
Perbedaan Senyawa dan molekul
“setiap senyawa adalah molekul namun setiap molekul belum tentu senyawa”. Senyawa adalah gabungan minimal 2 atom berbeda, sedangkan molekul gabungan minimal 2 atom bisa sama bisa juga berbeda.
Sumber: medlinkup.wordpress.com
AFINITAS ELEKTRON
Afinitas Elektron (electron affinity) yaitu negatif dari perubahan energi yang terjadi ketika satu elektron diterima oleh atom suatu unsur dalam keadaan gas. Afinitas elektron juga dinyatakan dalam kJ mol–1. Unsur yang memiliki afinitas elektron bertanda negatif, berarti mempunyai kecenderungan lebih besar dalam menyerap elektron daripada unsur yang afinitas elektronnya bertanda positif. Makin negatif nilai afinitas elektron, maka makin besar kecenderungan unsur tersebut dalam menyerap elektron (kecenderungan membentuk ion negatif). (Wikipedia)
Definisi Afinitas Elektron
Definisi Konvensional
Hampir semua atom netral mempunyai kapasitas untuk menerima paling tidak satu elektron tambahan, yang kemudian dikenal dengan istilah afinitas elektron. Pada proses ini umumnya dibebaskan energi, berlawanan dengan proses pengeluaran elektron dari suatu atom yang membutuhkan energi. Karena afinitas elektron menunjuk pada energi, maka lebih sering disebut sebagai energi afinitas (Ea). Secara konvensional, definisi energi afinitas adalah energi yang dibebaskan bila tiap mol atom netral atau ion dalam keadaaan gas menangkap elektron membentuk ion negatif. Dengan demikian, proses yang terjadi dapat dipandang sebagai kebalikan dari proses pelepasan elektron, yaitu :
M (g) + e
---> M-
.......... Ea(1)
M- (g) + e ---> M2- .......... Ea(2)
Dapat dipahami bahwa Ea(1) > Ea(2) > Ea(3) dan seterusnya, karena tambahan elektron kedua dan seterusnya akan mendapat tolakan dari spesies negatif hasil, sehingga tidak lagi dibebaskan energi melainkan malahan dibutuhkan energi yang semakin besar; dengan demikian energi yang dibebaskan semakin kecil atau bahkan negatif atau dengan kata lain justru membutuhkan energi.
M- (g) + e ---> M2- .......... Ea(2)
Dapat dipahami bahwa Ea(1) > Ea(2) > Ea(3) dan seterusnya, karena tambahan elektron kedua dan seterusnya akan mendapat tolakan dari spesies negatif hasil, sehingga tidak lagi dibebaskan energi melainkan malahan dibutuhkan energi yang semakin besar; dengan demikian energi yang dibebaskan semakin kecil atau bahkan negatif atau dengan kata lain justru membutuhkan energi.
Definisi Modern
Berlawanan
dengan perjanjian konvensional, publikasi para ahli kimia akhir-akhir ini
memandang afinitas elektron langsung dengan besaran termodinamika ∆H;
jadi, afinitas elektron didefinisikan sebagai perubahan entalpi yang terjadi
pada penambahan elektron ke dalam tiap mol atom atau ion dalam keadaan gas.
Misalnya untuk oksigen, afinitas elektron langsung diekspresikan dengan besaran
termodinamika sebagai berikut:
O (g) + e ---> O- (g) ∆H(1) = -141 kJ mol-1
O- (g) + e ---> O2- (g) ∆H(2) = +844 kJ mol-1
Dengan demikian perjanjian ini menghasilkan numerik yang sama tetapi berlawanan tanda dengan perjanjian konvensional untuk harga Ea. Untuk tidak menimbulkan kebingungan, maka yang perlu diperhatikan adalah harga dari besaran termodinamika dalam proses penangkapan elektron tersebut, karena kedua pandangan menghasilkan nilai yang sama. Oleh karena ∆H dapat positif atau negatif maka ungkapan data perlu dicantumkan bearan mana yang dipilih, seyogyanya ∆H.
O (g) + e ---> O- (g) ∆H(1) = -141 kJ mol-1
O- (g) + e ---> O2- (g) ∆H(2) = +844 kJ mol-1
Dengan demikian perjanjian ini menghasilkan numerik yang sama tetapi berlawanan tanda dengan perjanjian konvensional untuk harga Ea. Untuk tidak menimbulkan kebingungan, maka yang perlu diperhatikan adalah harga dari besaran termodinamika dalam proses penangkapan elektron tersebut, karena kedua pandangan menghasilkan nilai yang sama. Oleh karena ∆H dapat positif atau negatif maka ungkapan data perlu dicantumkan bearan mana yang dipilih, seyogyanya ∆H.
Kecenderungan Afinitas Elektron
Secara umum, kecenderungan afinitas elektron
dapat digeneralisasikan, walaupun dalam faktanya banyak yang menyimpang. Pada
unsur golongan 2 (alkali
tanah), mempunyai nilai afinitas elektron yang rendah. Unsur ini relatif
stabil karena telah menempati subkulit s. Golongan 17 (halogen)
mempunyai afinitas elektron yang tinggi karena adanya tambahan elektron pada
atom sebagai hasil dari pemenuhan orbital. Golongan 18 (gas mulia) mempunyai
afinitas elektron mendekati nol, karena masing-masing atom memperlihatkan
sebuah kestabilan oktet
dan tidak akan dapat menerima sebuah elektron lagi. Unsur dalam golongan lain
mempunyai afinitas yang lebih rendah. Berikut ini adalah contoh grafik
kecenderungan afinitas elektron:
Sumber: http://www.ilmukimia.org

Jari-Jari Atom
Jari-jari atom merupakan jarak
dari pusat inti ke elektron paling luar. Jari-jari atom ditemukan dengan
mengukur panjang ikatan atau jarak antar inti dalam senyawa karbon, Jari –jari
atom sering disebut jari-jari kovalen. Jari-jari atom berubah – ubah bergantung
pada besarnya tarikan antara inti dan elektronnya. Makin besar tarikan maka akan makin kecil jari-jari atomnya. Hal
ini dipengaruhi oleh jumlah proton dalam inti dan jumlah kulit yang mengandung
elektron.
Dalam kimia organik, atom
saling berikatan satu dengan yang lain dalam kedekatan yang dekat oleh ikatan
kovalen. Konsep jari-jari atom akan berguna dalam memperkirakan tarikan dan
tolakan antara atom dan dalam membahas kekuatan ikatan kovalen.
Keeloktronegatifan
Kelektronegatifan
merupakan ukuran kemampuan atom untuk menarik elektron luarnya atau elektron
valensi. Hal ini dikarenakan elektron
luar dari atom yang digunakan untuk ikatan , maka keelektronegatifan berguna
dalam meramalkan dan menerangkan
kereaktifan kimia. Kelektronegatifan ini dipengaruhi oleh jumlah proton dalam
inti dan jumlah kulit yang mengandung elektron. Makin besar jumlah proton
berarti makin besar muatan inti positif, dan dengan demikian tarikan untuk
elektron ikatan bertambah. Skala numeric dari keelektronegativan disebut dengan
skala pauling. Skala ini diturunkan dari perhitungan energy-ikatan untuk
berbagai unsure yang terikat oleh ikatan kovalen. Dalam skala pauling, flour, unsure
yang paling elektronegatif mempunyai nilai
4. Litium keelektronegatifannya rendah mempunyai elektronegatif 1. Sedangkan karbon memiliki
keelektronegatifan menengah 2,5.
Energy disosiasi
ikatan.
Bila atom saling terikat
membentuk molekul , energy dilepaskan (biasanya sebagai kalor atau cahaya). Jadu
untuk molekul agar terdiosiasi menjadi atom-atomnya, harus diberikan energy. Ada dua cara agar ikatan dapat
terdiosisasi. Satu cara adalah karena pemaksapisahan heterolitik (Heterolytic
Cleavage)( yunani hetero, “berbeda”) dimana kedua elektron ikatan dipertahankan
pada satu atom. Hasil dari pembelahan heterolik adalah sepasang ion. Proses
lain yang memungkinkan suatu ikatan terdisosiasi adalah pemaksa pisahan
homolitik(Yunani, homo, “sama”). Dalam hal ini setiap atom yang turut dalam
ikatan kovalen menerima satu elektron dari pasangan yang saling dibagi yang
asli. Yang dihasilkan adalah atom yang secara listrik netral atau gugus
atom. Pemaksapisahan homolitik menghasilkan atom atau gugus atom
yang mempunyai elektron yang berpasangan. Atom seperti H+ atau gugus atom seperti H3C yang
mengandung elektron tak berpasangan
disebut radikal bebas. Radikal bebas biasanya netral secara listrik
karena itu tak ada tarikan elektrostatik antara radikal bebas seperti ion. Energy
disosiasi ikatan memungkinkan ahli kimia untuk menghitung kesetabilan relative
dari senyawa dan meramaikan (sampai tariff tertentu) sebab-sebab reaksi kimia. Misalnya
suatu reaksi yang akan dibahas kemudian dalam teks ini adalah khlorinasi metana
CH4 :
CH4 + Cl2 ==> CH3Cl + HCl
TEORI ASAM-BASA

Dalam kesempatan ini pembahasan materi asam
basa ditekankan pada aspek teoritik untuk tingkah laku asam dan basa. Teori
asam basa sebagaimana umumnya terus berkembang untuk menjawab tantangan
berkaitan dengan teori-teori yang lebih awal. Teori asam basa yang paling
sederhana pada awalnya dikemukakan oleh Svante Arrhenius pada tahun 1884.
Menurut teori Arrhenius, asam adalah spesies yang mengandung ion-ion hidrogen,
H+ atau H3O+, dan basa mengandung ion
hidroksida (OH-). Namun demikian, dalam teori ini terdapat dua
kelemahan utama yang menyangkut masalah pelarut dan masalah garam.
Teori Asam Basa Arrhenius
Teori asam
basa Arrhenius didasarkan pada pembentukan ion dan pada larutan berair (aqueous
solution).
- Asam adalah spesies yang menghasilkan ion H+ atau H3O+ dalam larutan berair.
- Basa adalah spesies yang menghasilkan ion OH- dalam larutan berair.
Teori Asam Basa Lewis
Teori asam basa
Lewis didasarkan pada transfer pasangan elektron.
- Asam adalah spesies penerima (akseptor) pasangan elektron.
- Basa adalah spesies pemberi (donor) pasangan elektron.
Teori Asam Basa Brønsted-Lowry
Teori
asam basa Brønsted-Lowry didasarkan pada transfer proton.
- Asam adalah spesies pemberi (donor) proton.
- Basa adalah spesies penerima (akseptor) proton.
Sifat-sifat Asam Basa
Sifat Asam
- Mempunyai rasa asam (awas jangan sekali-sekali mencicipinya!). Kata asam berasal dari bahasa Latin acere yang berarti asam.
- Mengubah lakmus dari warna biru ke merah.
- Larutan asam menghantarkan arus listrik (bersifat elektrolit).
- Bereaksi dengan basa membentuk garam dan air.
- Menghasilkan gas hidrogen ketika bereaksi dengan logam (seperti logam alkali, alkali tanah, seng, aluminium).
Sifat Basa
- Mempunyai rasa pahit (awas jangan sekali-sekali mencicipinya!).
- Terasa licin atau bersabun (awas jangan secara langsung menyentuhnya!).
- Mengubah lakmus dari warna merah ke biru.
- Larutan basa menghantarkan arus listrik (bersifat elektrolit).
- Bereaksi dengan asam membentuk garam dan air.


6 comments
Write commentsSaya ingin menambahkan tentang Konsep asam dan basa dalam kimia organik
Reply1.Sifat Asam
Dari uraian mengenai asam yang telah dijelaskan di atas, sekarang kita akan membahas mengenai sifat asam dilihat dari sifat fisika maupun sifat kimia.
-Sifat Kimia Asam
Menurut penjelasan Arrhennius, jelas bahwa asam akan melepaskan kation Hidrogen (H+) jika terurai di dalam air, sedangkan menurut Brownstead - Lowry asam merupakan zat yang di dalam reaksinya akan mendonorkan proton (dalam hal ini akan mendonorkan kation). Sedangkan menurut Lewis, asam akan menerima pasangan elektron bebas yang diberikan oleh basa.
-Sifat Fisika Asam
Ditinjau dari sifat fisika, asam memang terasa masam walaupun tidak semua asam dapat dicicipi. Semua asam -Asam mineral bersifat korosif, yaitu mampu merusak dan dapat melarutkan permukaan logam dan lapisan kulit jika terkena kontak langsung. Inilah alasan mengapa asam akan menimbulkan sensasi tajam dan panas jika terkena kulit.
2.Sifat Basa
-Sifat Kimia Basa
Bisa dibilang basa adalah kebalikan dari asam. Basa, menurut Arrhennius, adalah zat yang akan membebaskan anion Hidroksida (OH-) jika dilarutkan di dalam air. Sedangkan menurut Brownstead - Lowry, basa adalah zat yang akan menerima donor proton (H+) dari asam, dan menurut Lewis basa akan mendonorkan pasangan elektron bebas kepada asam. Basa dapat menetralkan asam membentuk garam dan air. Larutan basa dapat merubah warna lakmus merah menjadi biru dan dapat merubah warna indikator PP dari tak berwarna (asam) menjadi merah (basa).
-Sifat Fisika Basa
Dilihat dari sifat fisikanya, basa memiliki rasa pahit walaupun basa tidak boleh dicicipi. Semua basa yang belum dibuat menjadi larutannya akan berbentuk padatan, kecuali NH4OH yang dari awal sudah berbentuk cairan. Jika kontak dengan kulit, basa akan terasa licin dan beberapa basa seperti NaOH dan KOH dapat menyebabkan iritasi dan gatal - gatal pada kulit. Basa juga sangat berbahaya bila kontak dengan selaput lendir seperti mata, oleh karena itu hati - hati ya!
Terimah kasih.
Terimakasih atas tambahan Materi tentang konsep asam dan basanya
Replysebelumnya izinkan saya menambahkan dari sumber yang saya baca tentang teori asam basa sifat asam basa pada larutan yang bebas air atau tidak mengandung air. Sebagai contoh, asam asetat akan bersifat asam jika dilarutkan dalam air, tetapi ternyata sifat asamtersebut tidak tampak pada saat asam asetat dilarutkan dalam benzena. Demikian juga dengan larutan amonia (NH3) dalam natrium amida (NaNH2) yang menunjukan sifat basa meskipun tidak mengandung ion OH–. Berdasarkan kenyataan tersebut, Johannes Bronsted dan Thomas Lowry secara terpisah mengusulkan bahwa yang berperan dalam memberikan sifat asam dan basa suatu larutan adalah ion H+ atau proton (ingat bahwa hidrogen hanya mempunyai sebuah elektron dan sebuah proton, jika elektronnya dilepaskan menjadi ion +1, yang tertinggal hanya proton saja).
ReplyMenurut teori asam basa Bronsted Lowry , asam adalah spesi (ion atau molekul) yang berperan sebagai donor proton (pemberi proton atau H+) kepada suatu spesi yang lain. Basa adalah spesi (molekul atau ion) yang bertindak menjadi akseptor proton (penerima proton atau H+).
Atau bisa juga dikatakan bahwa menurut teori asam basa Bronsted Lowry , jika suatu asam memberi proton (H+), maka sisa asam tersebut mempunyai kemampuan menerima proton atau bertindak sebagai basa. Sisa asam tersebut dinamakan basa konjugasi dari asam semula. Demikian pula, jika suatu basa menerima proton (H+), maka basa yang terbentuk mempunyai kemampuan untuk melepas proton tersebut atau bertindak sebagai asam konjugasi dari basa semula
assalamualaikum,
Replypostingan anda cukup baik disini saya tertarik pada keelektronegatifan , dimana Kelektronegatifan ini dipengaruhi oleh jumlah proton dalam inti dan jumlah kulit yang mengandung elektron. Makin besar jumlah proton berarti makin besar muatan inti positif, dan dengan demikian tarikan untuk elektron ikatan bertambah. Dalam skala pauling, flour, unsure yang paling elektronegatif mempunyai nilai 4. Litium keelektronegatifannya rendah mempunyai elektronegatif 1, hal ini menunjukkan bahwa semakin kekiri keelektronegatifan nya semakin rendah. nah yang ingin saya tanyakan bagaimana hubungan antara kelektronegatifan terhadap jar-jari atom, energi ionisasi, dan afinitas elektron terhadap muatan inti atom pada gaya tarik inti ke elektron terluar ?
Walaikumsalam terimakasih
ReplyUnsur-unsur dalam periode yang sama dari kiri ke kanan, muatan inti atom makin bertambah sehingga gaya tarik inti ke elektron terluar bertambah. Akibatnya, jari-jari atom makin kecil, energi ionisasi makin besar, afinitas elektron makin besar (makin negatif), dan kecenderungan untuk menarik elektron makin besar.
Potensial Ionisasi atau energi ionisasi adalah energi minimum yang diperlukan oleh suatu atom netral atau ion untuk melepas 1 buah elektron yang terikat paling luar dalam fase gas. Energi ionisasi dinyatakan dalam kJ mol–1. Semakin kecil jari-jari atom, potensial ionisasinya cenderung semakin besar. Hal ini karena semakin kecil jari-jari atom, akan semakin kuat suatu elektron ditarik oleh inti atom sehingga diperlukan energi yang lebih besar untuk melepaskan elektron tersebut.
Assalamu'alaikum ikhsan..
ReplyDari postingan anda diatas, saya ingin bertanya bisakah anda jelaskan Apa perbedaan affinitas elektron dan energi ionisasipa perbedaan affinitas elektron dan energi ionisasi?
Terima kasih
EmoticonEmoticon